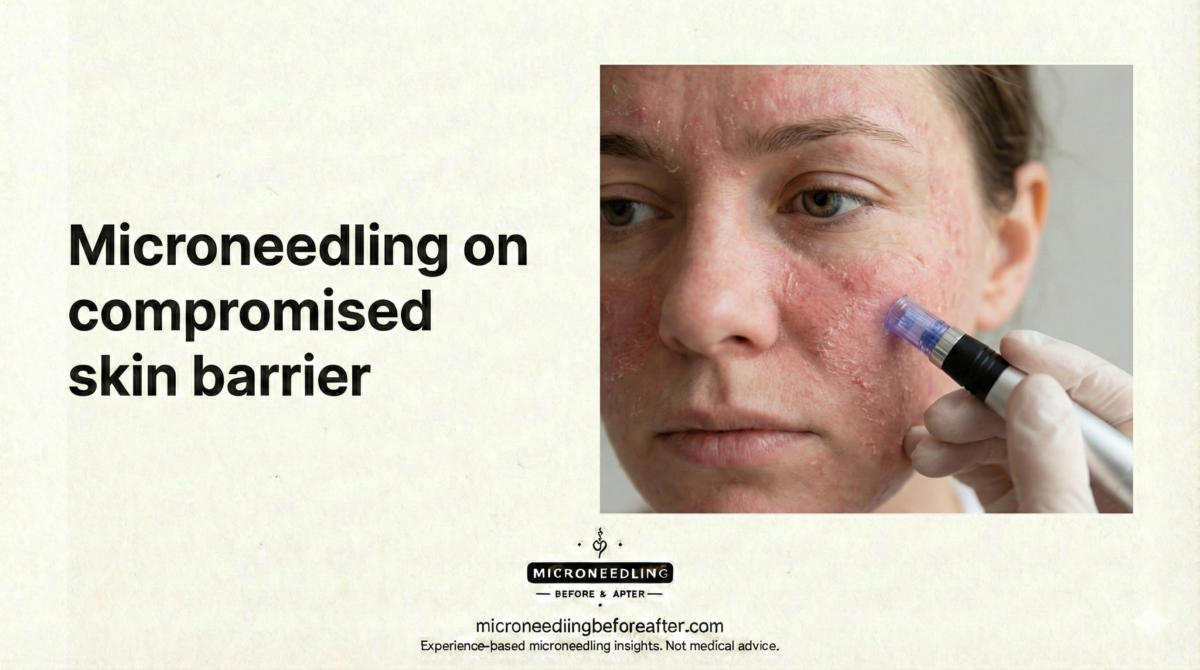
¿Es posible realizar microagujas de forma segura en piel que ya tiene una barrera comprometida y, de ser así, bajo qué condiciones y precauciones?
Microagujas en la barrera cutánea comprometida
Explicaré las intersecciones entre los procedimientos de microagujas y una barrera cutánea deteriorada, y brindaré una guía práctica y basada en la evidencia para la evaluación, la planificación del tratamiento y el cuidado posterior. Mi objetivo es brindar a profesionales clínicos, estéticos y pacientes informados un marco integral para la toma de decisiones seguras y la gestión de riesgos.
Por qué es importante este tema
Reconozco que la microaguja se usa ampliamente para mejorar la textura, las cicatrices y el tono, pero crea microlesiones controladas intencionalmente. Cuando la barrera cutánea se deteriora, estos microcanales alteran los perfiles de riesgo de infección, inflamación prolongada y desestabilización de la barrera. Por lo tanto, priorizaré la seguridad, los criterios claros de contraindicación y las estrategias para rehabilitar la barrera antes de cualquier intervención invasiva.
Fundamentos del estrato córneo y la función barrera
Revisaré brevemente la fisiología cutánea relevante para que las recomendaciones posteriores se basen en el mecanismo. El estrato córneo, los lípidos y los corneocitos proporcionan una barrera dinámica que controla la pérdida de agua transepidérmica, la defensa microbiana y la penetración química.
Las tres funciones principales que destaco son: prevenir la pérdida de agua, bloquear la entrada de patógenos y regular la penetración de agentes tópicos. Cuando estas funciones se ven comprometidas, se altera tanto el entorno inmunitario local como la capacidad de reparación de la piel, lo que afecta la respuesta a la microaguja.
¿Qué quiero decir con “barrera comprometida”?”
Utilizo el término “barrera comprometida” para describir la piel con integridad estructural reducida o fisiología alterada, lo que resulta en un aumento de la permeabilidad y una mayor sensibilidad. Las presentaciones clínicas típicas incluyen sequedad con fisuras, eritema y escozor, infecciones recurrentes e inflamación crónica.
Una barrera dañada puede ser transitoria (pospeeling químico, dermatitis aguda) o crónica (dermatitis atópica, daño prolongado por corticosteroides). La duración y la causa influyen en si la microaguja se pospone, modifica o considera tras la restauración.
Cómo funciona la microaguja y por qué es importante el estado de la barrera
Resumiré el mecanismo de la microaguja y lo relacionaré con sus implicaciones como barrera. Las microagujas crean microcanales que estimulan cascadas controladas de cicatrización, incluyendo la activación plaquetaria, la liberación de citocinas, el reclutamiento de fibroblastos y la remodelación del colágeno.
Estos mismos microcanales también eluden la barrera externa, lo que aumenta drásticamente la penetración tópica y permite la entrada de microbios si no se mantiene la esterilidad. En pieles con problemas de piel, la respuesta inflamatoria puede ser exagerada o desregulada, lo que aumenta la posibilidad de consecuencias adversas como inflamación persistente, infección, hiperpigmentación postinflamatoria y retraso en la cicatrización.
Profundidad, tipo de dispositivo y respuesta biológica
Explico que la longitud de la aguja, el tipo de dispositivo (rodillo, sello, bolígrafo) y la intensidad del tratamiento determinan la profundidad y la cantidad de tejido afectado. Considero que las agujas más cortas (<0,5 mm) en su mayoría epidérmicos y agujas más largas (>1,5 mm) dérmico.
En pieles con problemas, incluso las agujas más cortas pueden provocar una reactividad no deseada, ya que la epidermis puede estar ya fina o inflamada. Recomiendo adaptar la técnica a la profundidad mínima efectiva y considerar alternativas no invasivas mientras la barrera se recupera.
Causas comunes de una barrera cutánea comprometida
Enumeraré y describiré los factores contribuyentes comunes para que los lectores puedan identificar situaciones relevantes. Los factores incluyen dermatosis inflamatorias, daño iatrogénico, agresiones ambientales, uso excesivo de productos decapantes e infecciones.
- La dermatitis atópica y las afecciones eccematosas crónicas reducen el contenido lipídico y alteran la señalización inmunitaria.
- El uso excesivo de exfoliantes (AHA, BHA, retinoides, exfoliantes físicos) puede provocar la destrucción de la barrera cutánea.
- El uso indebido de corticosteroides tópicos puede adelgazar la epidermis y perjudicar los mecanismos de reparación.
- Los procedimientos faciales recientes (peelings químicos, láser, microdermoabrasión agresiva) dejan la barrera extremadamente vulnerable.
- La infección activa (herpes simple, impétigo) representa una clara contraindicación hasta que se resuelva.
Signos y síntomas que indican compromiso de la barrera
Quiero que puedas reconocer los indicadores de la consulta. Busca escozor o ardor al aplicar productos benignos, sequedad persistente con descamación, eritema mayor al basal, fisuras visibles, infecciones recurrentes e hiperreactividad a los ingredientes tópicos. Medidas objetivas como la pérdida de agua transepidérmica (TEWL) y la corneometría respaldan la evaluación cuando estén disponibles.
Si detecto signos agrupados, especialmente infección activa o atrofia inducida por corticoides, categorizaré la barrera como comprometida y evitaré la punción hasta la recuperación.
Riesgos de realizar microagujas en pieles comprometidas
Describiré los principales riesgos y explicaré sus mecanismos. Entre ellos se incluyen infección, inflamación prolongada, cicatrización, cambios pigmentarios, sensibilidad crónica y exacerbación de dermatosis subyacentes.
Infección: Los microcanales evitan las capas protectoras, lo que permite que los patógenos colonicen la dermis si la asepsia es imperfecta o el microbioma residente está desequilibrado.
Inflamación y cicatrización: una respuesta exagerada o desregulada de la herida en la piel comprometida puede provocar cicatrices hipertróficas o una curación tardía.
Pigmentación: La hiperpigmentación postinflamatoria (HPI) es más probable cuando hay inflamación basal, en particular en los tipos de piel con un índice Fitzpatrick superior.
Exacerbación: Afecciones como la rosácea o el eczema pueden reaparecer después del procedimiento, prolongando la recuperación y potencialmente causando la necesidad de esteroides sistémicos.
Contraindicaciones relativas versus absolutas
Clasifico las contraindicaciones en absolutas (condiciones que deberían excluir el procedimiento) y relativas (condiciones que requieren modificación o aplazamiento). Las contraindicaciones absolutas incluyen infección activa (VHS, bacteriana), brotes de enfermedades autoinmunes no controlados, uso activo de isotretinoína dentro del intervalo de seguridad recomendado y procedimientos ablativos recientes. Las contraindicaciones relativas incluyen eccema leve en remisión, uso reciente de esteroides tópicos sin atrofia y antecedentes de mala cicatrización de heridas o tendencia a queloides; estas requieren una evaluación individualizada.
Evaluación previa al procedimiento y toma de decisiones
Proporcionaré una lista de verificación que utilizo antes de ofrecer microagujas. Es fundamental obtener una historia clínica completa, un examen de la piel y una evaluación de riesgos y beneficios. Evalúo el historial médico (dermatitis atópica, rosácea), los procedimientos recientes, la medicación tópica/sistémica actual, los signos de infección y las expectativas del paciente.
Documento el estado basal de la piel, incluyendo eritema, descamación, fisuras y cualquier zona de atrofia. En caso de duda, pospongo el procedimiento o realizo una prueba conservadora en la zona para observar la reactividad inmediata.
Lista de verificación de evaluación práctica (tabla)
Incluyo una tabla para aclarar los elementos que reviso rutinariamente antes de realizar la microaguja.
| Elemento de evaluación | Lo que busco | Acción si es positiva |
|---|---|---|
| Infección activa (VHS, impétigo) | Vesículas, costras, dolor. | Aplazar hasta que se resuelva; antivirales/antibióticos según esté indicado |
| Uso reciente de isotretinoína | Isotretinoína en un plazo de 6 a 12 meses | Aplazar según las pautas de práctica |
| Atrofia relacionada con esteroides tópicos | Adelgazamiento, telangiectasias, facilidad para hematomas | Aplazar o limitar a terapias no invasivas; derivar |
| Actividad de eczema/psoriasis | Eritema, descamación, prurito | Tratar y estabilizar antes de la punción. |
| Renovación agresiva reciente | Descamación de la piel, heridas abiertas | Aplazar hasta la reepitelización completa |
| Tipo de piel del paciente | Clasificación de Fitzpatrick e historia de la HIP | Modificar la profundidad; asesorar sobre el riesgo de PIH |
| Expectativas y adherencia del paciente | Comprensión del tiempo de inactividad y cuidados posteriores | Educar; obtener el consentimiento |
Estrategias clínicas al considerar la microaguja en piel marginalmente comprometida
Describiré cómo modifico las técnicas cuando la barrera está ligeramente deteriorada y la microaguja sigue siendo adecuada. Mis objetivos son minimizar el trauma, reducir el riesgo de infección y favorecer la rápida restauración de la barrera.
- Reducir la profundidad de la aguja y la intensidad de la sesión; preferir 0,25–0,5 mm para la estimulación epidérmica.
- Ampliar los intervalos entre sesiones para permitir una recuperación más completa.
- Utilice cartuchos estériles de un solo uso y una técnica aséptica estricta.
- Evite realizar rejuvenecimiento químico o físico complementario en la misma sesión.
- Considere agentes tópicos que promuevan la reparación de la barrera, pero evite aquellos que sean altamente permeables y potencialmente irritantes.
Cuándo utilizar anestésicos tópicos y sueros
Soy cauteloso con los anestésicos tópicos, ya que pueden contener alcohol o conservantes que alteran aún más la barrera protectora. Si es necesario usar anestésicos tópicos, utilizo fórmulas sin conservantes y minimizo el tiempo de contacto. Para los sérums, selecciono fórmulas estériles y sencillas (factores de crecimiento o ácido hialurónico en vehículos estériles y sin conservantes) solo si la piel no presenta signos de infección activa.
Cuidados posteriores: rehabilitación de la barrera
Doy mucha importancia al cuidado posterior para la reparación de la barrera cutánea. Mis prioridades son: mantener la hidratación, prevenir infecciones, minimizar la inflamación y evitar irritantes. Indico a mis pacientes que utilicen limpiadores suaves sin perfume, emolientes oclusivos y protector solar.
Recomiendo aplicar un humectante (p. ej., ácido hialurónico) en capas con un oclusivo (p. ej., vaselina o ungüento rico en ceramidas) para retener la hidratación. El protector solar es esencial, ya que la exposición a los rayos UV puede empeorar la hiperpigmentación cutánea y retrasar la reparación epidérmica.
Cronograma detallado de cuidados posteriores
Ofrezco un cronograma práctico que prefiero para sesiones sencillas que se puedan ajustar para pieles comprometidas.
- Inmediato (0-12 horas): Limpieza suave con solución salina estéril o un limpiador suave; aplicar suero hialurónico estéril sin conservantes si se tolera y, a continuación, emoliente oclusivo. Evitar el maquillaje.
- 12 a 72 horas: Continuar con una limpieza suave dos veces al día, usar emolientes frecuentes, evitar ingredientes activos (retinoides, ácidos), usar FPS físico o mineral una vez reepitelizado.
- Día 3–14: Reintroducción gradual de activos que apoyan la barrera (niacinamida, ceramidas); volver a activos más fuertes solo después de la recuperación total de la barrera y la autorización del médico.
- Continuo: Enfatizar el cuidado regular de la piel que apoya la barrera cutánea y la protección solar.
Ingredientes y selección de productos: lo que uso y lo que evito
Considero que una lista clara de ingredientes recomendados y contraindicados ayuda a reducir la confusión. Enfatizo en el uso de fórmulas estériles, no irritantes y que reparen la barrera cutánea, y en evitar el alcohol, las fragancias, los ácidos de alta concentración y los agentes potencialmente fotosensibilizantes.
Lista de recomendaciones y de evitar (tabla)
Esta tabla resume los ingredientes comunes que recomiendo o evito en la ventana perioperatoria inmediata.
| Usar inmediatamente después del procedimiento. | Evitar inmediatamente después del procedimiento. |
|---|---|
| Ácido hialurónico estéril (bajo peso molecular) | Tónicos que contienen alcohol |
| Petrolato o ungüentos oclusivos | AHA/BHA de alta potencia |
| Cremas ricas en ceramidas | Retinoides (durante 7 a 14 días) |
| Niacinamida (después de 48 a 72 horas si se tolera) | Peróxido de benzoilo (irritante) |
| Limpiadores suaves y sin fragancia | Exfoliantes |
| Protector solar mineral una vez reepitelizado | Protectores solares químicos con potencial irritación si la piel reacciona |
Opciones de dispositivos: clínica profesional versus unidades domiciliarias
Siempre recomiendo precaución con los dispositivos de microagujas para uso doméstico, especialmente en pieles con problemas. Los dispositivos profesionales ofrecen profundidades controladas, cartuchos estériles desechables y se aplican en un entorno aséptico por profesionales cualificados.
Los rodillos caseros suelen carecer de un control de profundidad constante, pueden reutilizarse entre sesiones y aumentan el riesgo de microtraumatismos e infecciones. Si los pacientes insisten en el mantenimiento en casa, recomiendo agujas cortas (<0,25 mm), higiene rigurosa y solo después de la recuperación completa de la barrera.< />>
Tabla comparativa: microagujas en clínica vs. en casa
Proporciono una comparación simple para aclarar las diferencias y consideraciones de seguridad.
| Característica | Microagujas en clínica | Microagujas en casa |
|---|---|---|
| Control de profundidad de la aguja | Preciso, ajustable | A menudo fijo, inconsistente |
| Esterilidad | Cartuchos estériles de un solo uso, técnica aséptica entrenada | Dispositivos reutilizables, limpieza variable |
| Evaluación clínica | Es posible realizar una evaluación previa al procedimiento | Solo autoevaluación |
| Capacidad para tratar complicaciones | Atención profesional inmediata | Retrasar la búsqueda de ayuda puede empeorar los resultados |
| Idoneidad para pieles comprometidas | Condicional con modificaciones | Generalmente desaconsejado |
Contraindicaciones y poblaciones especiales
Indico contraindicaciones claras y consideraciones especiales para pacientes con ciertas afecciones sistémicas. Las contraindicaciones absolutas incluyen infección cutánea activa, isotretinoína reciente dentro de un plazo seguro, brotes de enfermedades autoinmunes no controladas, antecedentes de queloides con tendencia a la cicatrización activa y embarazo para algunos dispositivos o accesorios.
En pacientes inmunodeprimidos o que reciben esteroides sistémicos, procedo con extrema precaución o recurro a terapias alternativas. Para pieles más oscuras (tipo Fitzpatrick), brindo asesoramiento exhaustivo sobre el riesgo de HIP y considero enfoques conservadores o modalidades alternativas con menor potencial inflamatorio.
Embarazo, lactancia y medicamentos
Explico que, si bien la microaguja en sí no está contraindicada universalmente durante el embarazo, los agentes tópicos adyuvantes, los anestésicos locales y los procedimientos asociados pueden estarlo. Evalúo cada caso individualmente y, a menudo, pospongo la microaguja cosmética electiva durante el embarazo o la lactancia hasta después de consultar con el obstetra.
Los medicamentos como los retinoides sistémicos requieren períodos de lavado establecidos; yo me adhiero a los intervalos recomendados por las guías para reducir los riesgos de cicatrización tardía y cicatrices.
Manejo de las complicaciones: detección temprana y tratamiento
Describo un enfoque algorítmico que utilizo para las complicaciones más comunes. El reconocimiento rápido previene la escalada.
- Infección: si aparece eritema local, dolor creciente, purulencia o síntomas sistémicos, inicio antibióticos tópicos o sistémicos dirigidos por cultivo y considero una incisión/drenaje si se forma un absceso.
- Reactivación del herpes simple: en pacientes con HSV positivo conocido, los antivirales profilácticos alrededor del procedimiento reducen el riesgo; trate los brotes activos con antivirales sistémicos y posponga la punción.
- Inflamación/brote persistente: trato con estrategias antiinflamatorias tópicas (esteroides de baja potencia a corto plazo si está indicado, o antiinflamatorios no esteroides como inhibidores tópicos de la calcineurina en algunos escenarios), guiados por el dermatología cuando es necesario.
- PIH: Uso temprano de protección solar, agentes aclaradores tópicos después de la reepitelización (ácido azelaico, niacinamida) y evitar traumatismos posteriores. Si persiste, puedo derivar a terapias pigmentarias dirigidas.
Cuándo derivar a dermatología o atención especializada
Soy rápido en derivar pacientes si hay alguna duda sobre la cicatrización, evidencia de infección grave, cicatrices inesperadas o síntomas sistémicos. Para afecciones dermatológicas complejas (p. ej., dermatitis atópica grave, enfermedades ampollosas autoinmunes), coordino la atención y prefiero horarios y protocolos guiados por el dermatólogo.
Protocolos de rehabilitación para restaurar la barrera pre-procedimiento
Ofrezco un plan basado en la evidencia para la rehabilitación de una barrera cutánea dañada antes de cualquier microaguja electiva. El objetivo es lograr una mejora objetiva de la hidratación, reducir la inflamación y normalizar la pérdida de agua transesofágica (TEWL) cuando sea posible.
- Curso corto de emolientes tópicos ricos en ceramidas y colesterol para reconstruir la matriz lipídica.
- Reducir o pausar el uso de exfoliantes activos y retinoides durante 2 a 4 semanas o hasta que se recupere la tolerancia.
- Si la dermatosis inflamatoria está activa, trate con terapias dirigidas (esteroides tópicos, inhibidores de la calcineurina o agentes sistémicos según esté indicado) hasta controlarla.
- Considere realizar una prueba de parche o reintroducir supervisadamente los principios activos sensibilizadores cuando el paciente esté listo.
Generalmente espero al menos 2 a 6 semanas de mejoría clínica documentada antes de reconsiderar la aplicación de agujas, con intervalos más largos para afecciones graves o crónicas.
Ejemplo práctico de producto y régimen
Suelo recomendar: una limpieza suave dos veces al día, la aplicación inmediata de un sérum humectante después de la limpieza, una crema espesa rica en ceramidas por la mañana y por la noche, y vaselina oclusiva por la noche durante una o dos semanas. Monitoreo los signos clínicos semanalmente y reevalúo la preparación mediante una lista de verificación que incluye la ausencia de inflamación activa, la reducción de los síntomas de TEWL y una mejor tolerancia.
Resumen de la evidencia y lagunas de conocimiento
Resumo la evidencia clave, reconociendo las limitaciones. Estudios clínicos demuestran que la microaguja trata eficazmente las cicatrices y el fotoenvejecimiento, con perfiles de seguridad generalmente favorables en piel sana. Sin embargo, existe escasa evidencia de alta calidad que aborde específicamente los resultados en casos de deterioro preexistente de la barrera cutánea.
Los ensayos aleatorizados rara vez incluyen pacientes con dermatitis activa o lesión reciente de la barrera cutánea; por lo tanto, las recomendaciones suelen derivar del razonamiento basado en mecanismos, el consenso de expertos y estudios observacionales más pequeños. Por lo tanto, practico modificaciones conservadoras y priorizo la evaluación individualizada.
Áreas que necesitan más investigación
Identifico lagunas de investigación relevantes desde el punto de vista clínico, como ensayos controlados aleatorizados sobre la seguridad de la microaguja en la disfunción de barrera leve a moderada, la configuración óptima del dispositivo para pieles con problemas y el papel de los adyuvantes específicos para la reparación de la barrera en la mejora de los resultados.
Recomendaciones prácticas: resumen paso a paso
Ofrezco un enfoque conciso y paso a paso que pueden aplicar los médicos o los pacientes informados.
- Evalúe exhaustivamente el estado de la barrera y documente los hallazgos.
- Clasificar el riesgo: contraindicación absoluta, contraindicación relativa o aceptable con modificaciones.
- Si está marginalmente comprometida, rehabilitar la barrera con emolientes y terapia antiinflamatoria hasta mejorar.
- Si continúa, utilice profundidades de aguja conservadoras, una técnica estéril y cartuchos de un solo uso.
- Evite combinar con otros tratamientos de resurfacing en la misma sesión.
- Utilice emolientes y oclusiones estériles y suaves después del procedimiento; evite los irritantes.
- Vigile de cerca si hay infección, inflamación prolongada o cambios pigmentarios y actúe de forma temprana.
- Para cualquier duda o complicación consulte a dermatología.
Escenarios de casos para ilustrar la aplicación
Presento breves casos hipotéticos para aplicar principios.
Caso 1: Una persona de 35 años con eccema leve, bien controlado con emolientes, solicita microagujas para las cicatrices del acné. Trato y estabilizo el eccema durante 4 a 6 semanas, confirmo la remisión clínica y luego procedo con microagujas poco profundas y con intervalos de recuperación más largos.
Caso 2: Un paciente de 28 años que usó isotretinoína tópica hace dos meses acude para una punción. La aplazo hasta que transcurra el periodo de reposo recomendado (normalmente de 6 a 12 meses, según la dosis y las directrices) debido al riesgo de cicatrización.
Caso 3: Una mujer de 45 años con una exfoliación química reciente y descamación visible solicita combinar tratamientos. Pospongo la microaguja hasta la reepitelización completa para evitar agravar la lesión de la barrera cutánea y el riesgo de infección.
Consideraciones finales y conclusión
Priorizo la seguridad del paciente y unas expectativas de resultados realistas. La microaguja puede ser valiosa, pero no está exenta de riesgos cuando la barrera cutánea está comprometida. Los profesionales sanitarios deben equilibrar la intención terapéutica con un enfoque conservador y basado en la evidencia que priorice la restauración de la barrera cutánea, la técnica aséptica, la configuración individualizada del dispositivo y un seguimiento minucioso.
Recomiendo documentar la asesoría, realizar una evaluación exhaustiva previa al procedimiento y evitar atajos con dispositivos caseros en pieles comprometidas. En caso de duda, prefiero retrasar el procedimiento y restaurar la barrera protectora en lugar de tratar complicaciones prevenibles.
Si lo desea, puedo proporcionarle una lista de verificación previa al procedimiento imprimible, un régimen de rehabilitación personalizado basado en un escenario clínico específico o referencias a pautas clínicas que uso en la práctica.