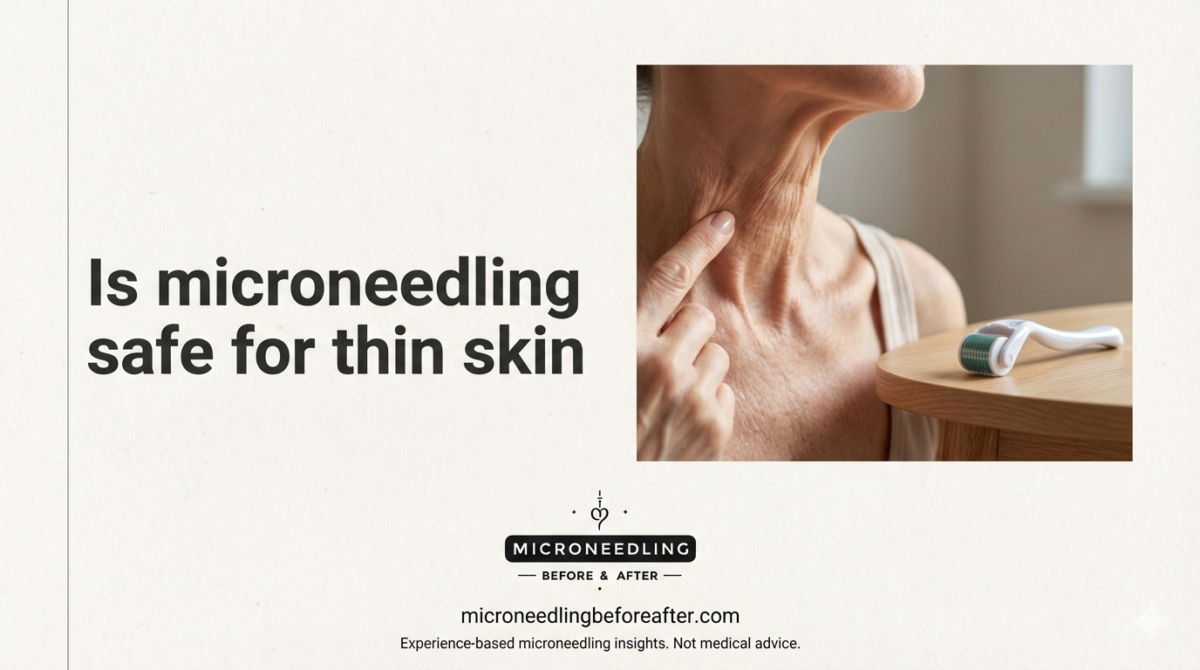
¿Pongo en riesgo mi piel fina si pruebo la microaguja, o puedo obtener sus beneficios de forma segura sin comprometer mi barrera cutánea?
¿Es segura la microaguja para la piel fina?
Me hacen esta pregunta con frecuencia y quiero explicarla con detalle para que puedas tomar una decisión informada. Te explicaré qué hace la microaguja, por qué es importante tener la piel fina y cómo elaborar un plan seguro si decides hacerlo.
¿Qué es la microaguja?
La microaguja es un procedimiento que utiliza agujas diminutas para crear microlesiones controladas en la piel. Lo considero una forma de estimular la respuesta reparadora natural de la piel (la producción de colágeno y elastina), en lugar de un rejuvenecimiento agresivo.
Cómo funciona la microaguja
Cuando las agujas perforan la piel, el trauma controlado desencadena la inflamación, seguida de la remodelación tisular y la síntesis de colágeno. Me resulta útil recordar que el objetivo es la reparación controlada: las agujas son lo suficientemente superficiales como para evitar daños mayores, pero lo suficientemente profundas como para activar los mecanismos de curación.
¿Qué quiero decir con “piel fina”?”
Cuando hablo de piel fina, me refiero a piel con menor grosor dérmico, a menudo con mayor translucidez, vasos sanguíneos visibles, arrugas finas y una textura de aspecto frágil. La piel fina puede ser un rasgo natural, resultado del daño solar, la pérdida de colágeno relacionada con la edad, el uso prolongado de esteroides tópicos o ciertas afecciones médicas.
Por qué la piel fina es importante para la microaguja
La piel fina tiene menos amortiguación y menos proteínas estructurales, por lo que puede responder de forma diferente y lesionarse con mayor facilidad con procedimientos mecánicos. Trato los casos de piel fina con especial precaución, ya que el riesgo de enrojecimiento prolongado, hematomas o incluso cicatrices atróficas puede ser mayor.
Beneficios de la microaguja para pieles finas
Los principales beneficios de la microaguja (estimular el colágeno y mejorar la textura) también se pueden aplicar a la piel fina, y muchas personas con piel fina reportan resultados más suaves y firmes con el transcurso de los tratamientos. He visto a clientes con piel fina beneficiarse, especialmente cuando la microaguja se adapta (profundidad de aguja menor, intervalos más largos) y se combina con cuidados posteriores protectores.
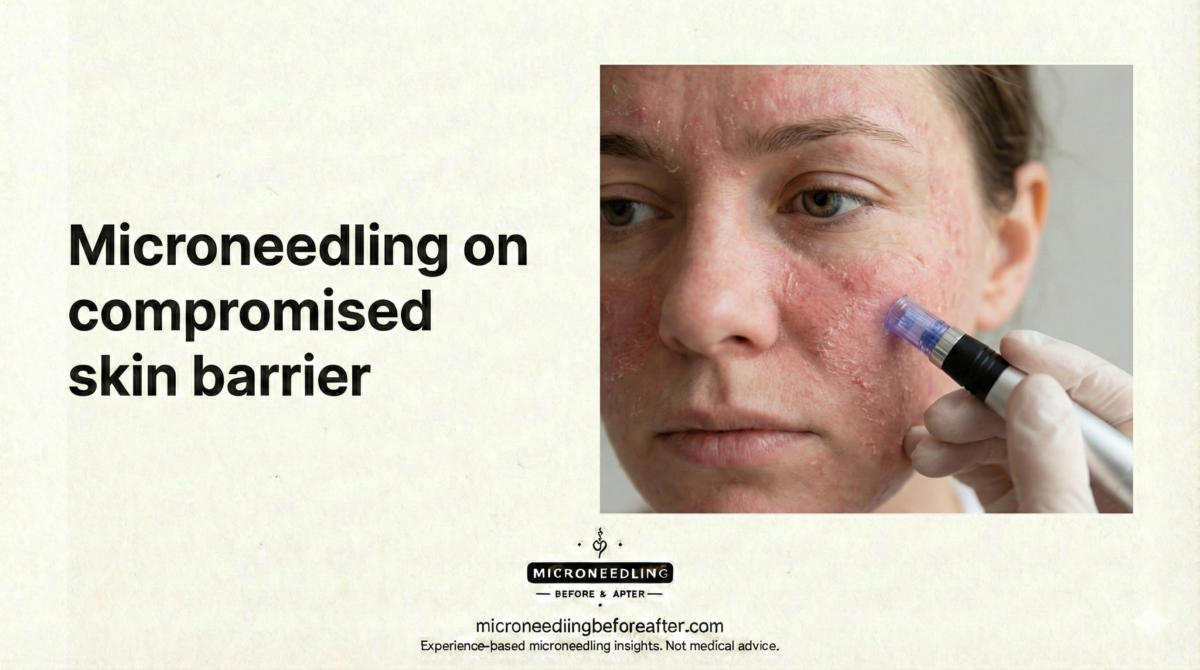
Riesgos y complicaciones específicos de la piel fina
Los riesgos que más me preocupan son el eritema prolongado (enrojecimiento), la púrpura (moretones), la sensibilidad persistente, la rotura de capilares y, en casos excepcionales, la cicatrización atrófica o la hiperpigmentación. También estoy atento a la mala cicatrización de heridas en personas con afecciones subyacentes, y enfatizo que incluso un riesgo de infección leve es más grave cuando la barrera cutánea es frágil.
Complicaciones típicas y cómo se manifiestan
Las complicaciones menores incluyen enrojecimiento, sangrado localizado, hinchazón y sensibilidad temporal que suele resolverse en días. Las complicaciones graves o persistentes (cicatrices, hiperpigmentación prolongada o infección significativa) son poco frecuentes, pero pueden ser más problemáticas en pieles finas si no se tratan con prontitud.
Cómo se mide el grosor de la piel
Los dermatólogos o profesionales sanitarios suelen estimar el grosor de la piel clínicamente mediante inspección y palpación, y se puede realizar una medición más precisa mediante ecografía o imágenes de alta resolución. Recomiendo una evaluación objetiva cuando la piel se ve inusualmente delgada o cuando se presentan el uso de esteroides u otros factores de riesgo.
Causas de la piel fina que busco
Siempre pregunto sobre el uso prolongado de esteroides tópicos o sistémicos, la exposición solar significativa, el envejecimiento, los antecedentes médicos (como trastornos del tejido conectivo) y el historial de procedimientos cosméticos. Considero que abordar las causas reversibles y optimizar la salud de la piel antes de la microaguja reduce la probabilidad de complicaciones.
¿Quién debería evitar la microaguja?
Aconsejo posponer o evitar la microaguja si se presentan infecciones cutáneas activas, acné severo, tendencia a queloides, diabetes no controlada, uso reciente de isotretinoína (en los últimos 6 a 12 meses en muchos protocolos) o trastornos de la coagulación sin tratar. Si sospecho que la piel fina se debe al abuso de esteroides o a un problema sistémico subyacente, es importante que se gestionen primero esos factores.
Microagujas profesionales vs. dispositivos para uso doméstico
Prefiero la microaguja profesional para personas con piel fina, ya que los profesionales pueden ajustar la profundidad y la técnica de la aguja, además de usar protocolos estériles que reducen el riesgo de complicaciones. Los rodillos y bolígrafos caseros suelen tener agujas menos profundas, pero conllevan riesgos de infección y de técnica; soy cauteloso al recomendarlos para pieles frágiles.
Tabla: Microagujas profesional vs. en casa: consideraciones para pieles finas
| Característica | Microagujas profesional | Derma-Rollers / Plumas para uso doméstico |
|---|---|---|
| Control de profundidad de la aguja | Preciso, ajustable (0,25–3,0 mm) | Generalmente menos profundo, control variable |
| Esterilidad | Realizado en condiciones estériles | Mayor riesgo de contaminación |
| Evaluación del proveedor | Preselección y protocolo personalizado | Sin evaluación profesional |
| Control del dolor | Anestesia tópica opcional | Control limitado del dolor |
| Supervisión posterior al cuidado | Seguimiento profesional | Autogestionado |
| Seguridad para pieles finas | Más seguro cuando lo ajusta un profesional | Mayor riesgo si se hace un mal uso |
Profundidad y ajustes de la aguja: recomendaciones para pieles finas
Para pieles finas, recomiendo profundidades de aguja conservadoras, generalmente entre 0,25 mm y 0,5 mm para una mejora estética sin traumatismo dérmico profundo. Si un profesional considera un tratamiento más profundo (0,75–1,5 mm), espero una justificación clara y un proceso de selección de pacientes muy cuidadoso, a veces comenzando con puntos de prueba.
¿Cuántas sesiones y espaciamiento recomiendo habitualmente?
Suelo sugerir una serie inicial de 3 a 6 sesiones con un intervalo de 4 a 8 semanas, según la respuesta y la tolerancia. Para pieles finas, suelo aumentar el intervalo entre sesiones para permitir una recuperación completa y controlar las reacciones adversas tardías.
Recomiendo la evaluación y las pruebas previas al tratamiento.
Antes de aceptar la microaguja, elaboro mi historial médico y farmacológico completo, evalúo el estado de la piel, busco signos de adelgazamiento y, en ocasiones, solicito una consulta con un dermatólogo o una ecografía en casos de incertidumbre. Si he usado isotretinoína o esteroides sistémicos recientemente, pospongo el tratamiento según las pautas de seguridad.
Preparación de la piel antes de la microaguja
Recomiendo mejorar la función de barrera cutánea antes del procedimiento: suspender los activos irritantes (como retinoides y exfoliantes) durante una semana o más, mantener la hidratación con cremas hidratantes suaves y usar protección solar. A veces recomiendo sérums tópicos sin factor de crecimiento e ingredientes que fortalezcan la barrera cutánea, pero evito introducir demasiados productos nuevos justo antes de una sesión.
El procedimiento: qué sucede durante una sesión
Durante una sesión profesional, el profesional limpiará la piel, aplicará anestesia tópica si es necesario y pasará una aguja estéril por la zona a tratar con movimientos controlados. Les recuerdo que es normal que se presenten puntos de sangrado leves y enrojecimiento reciente, y que el profesional debe ejercer una presión suave y la configuración adecuada para pieles finas.
Dolor, anestesia y medidas de confort.
Suelo usar anestesia tópica para mayor comodidad cuando se requieren tratamientos más profundos, y explico que los tratamientos menos profundos pueden causar solo un ligero escozor. También sugiero medidas para aliviar el estrés, como ejercicios de respiración y distracción, ya que una menor ansiedad puede mejorar la tolerancia y reducir los movimientos involuntarios.
Cuidados posteriores y recuperación para pieles finas
Mis recomendaciones para el cuidado posterior se centran en proteger la barrera cutánea dañada: limpieza suave, cremas hidratantes sin perfume y protector solar de amplio espectro, comenzando inmediatamente cuando la piel deja de supurar. Aconsejo a los pacientes evitar exfoliantes, ingredientes activos (retinoides, ácidos), saunas y ejercicio intenso durante varios días para limitar el riesgo de irritación e infección.
El tiempo típico de recuperación que analizo
En la mayoría de los casos, el enrojecimiento y la tirantez mejoran en 48 a 72 horas, con una mejora continua durante una semana. Les digo a mis pacientes que esperen algún cambio en la textura y una ligera descamación hasta por dos semanas. En pieles finas, controlo si el enrojecimiento o la sensibilidad persisten y ajusto la frecuencia de las sesiones posteriores según corresponda.
Manejo de complicaciones si ocurren
Si observo signos de infección (dolor creciente, pus, fiebre), solicito atención médica inmediata y suelo iniciar el tratamiento con antibióticos adecuados. En caso de enrojecimiento prolongado, hematomas o hiperpigmentación postinflamatoria, considero el uso de antiinflamatorios tópicos, terapias basadas en luz y tratamientos dirigidos a la pigmentación una vez que la barrera cutánea es adecuada.
Tabla: Complicaciones comunes y mis intervenciones típicas
| Complicación | Periodo de tiempo | Intervención que recomiendo |
|---|---|---|
| Enrojecimiento prolongado | >7–14 días | Tópicos antiinflamatorios, enfriamiento, observación prolongada. |
| hematomas/púrpura | 1–2 semanas | Compresas frías inicialmente; tiempo y evitar anticoagulantes. |
| Infección | En cualquier momento después del procedimiento | Evaluación urgente; antibióticos tópicos/sistémicos según sea necesario. |
| Hiperpigmentación | Semanas a meses | Protección solar, agentes blanqueadores tópicos o terapia de luz. |
| Cicatrización | Semanas–meses | Derivación temprana a dermatología; esteroides intralesionales para cicatrices hipertróficas |
Microagujas en casa: ¿vale la pena el riesgo para la piel fina?
Rara vez recomiendo herramientas de microagujas caseras para piel fina debido a la variabilidad en la calidad de las agujas, la higiene y la técnica. Si alguien insiste, exijo instrucciones estrictas: longitud segura de la aguja (≤0,25–0,3 mm), esterilización rigurosa y suspensión inmediata del tratamiento si se produce enrojecimiento o sangrado excesivos.
Combinando microagujas con PRP o sueros tópicos
He visto la microaguja combinada con plasma rico en plaquetas (PRP) o sueros tópicos para mejorar la cicatrización y la estimulación del colágeno, pero soy cauteloso al combinar productos biológicos activos en pieles finas sin datos de seguridad claros. Si se usa PRP, prefiero que se prepare y aplique en condiciones estériles y a poca profundidad; en cuanto a los sueros tópicos, elijo aquellos que favorecen la reparación de la barrera cutánea en lugar de aumentar la inflamación.
Momento después de otros procedimientos cosméticos
Pospongo la microaguja después de tratamientos con láser, peelings químicos o cirugías hasta que la piel haya cicatrizado por completo. También espero los intervalos adecuados después de inyecciones de relleno o tratamientos con neuromoduladores, a menos que el profesional tenga experiencia en combinar modalidades de forma segura.
Alternativas para piel fina que considero
Cuando la microaguja parece arriesgada, considero opciones más suaves para estimular el colágeno: peelings químicos de baja potencia, péptidos tópicos, retinoides recetados en dosis controladas, terapias de luz (LED, láseres de baja energía) y cosmecéuticos para reconstruir la matriz dérmica. En ocasiones, también recomiendo inyecciones para estimular el colágeno o rellenos bioestimulantes, aplicados de forma muy conservadora.
Tabla: Alternativas a la microaguja: ventajas y desventajas para pieles finas
| Tratamiento | Ventajas | Contras |
|---|---|---|
| Terapia de luz LED | No invasivo, reduce la inflamación y favorece la curación. | Resultados más lentos y leves |
| Peelings químicos de baja potencia | Puede mejorar la textura con una exfoliación controlada. | Riesgo de irritación si la piel es muy fina. |
| Retinoides tópicos (dosis baja) | Estimula el colágeno con un uso cuidadoso. | Puede irritar inicialmente y debilitar la barrera si se usa incorrectamente. |
| PRP solo (sin microagujas) | Factores de crecimiento autólogos, menor trauma mecánico | Prueba variable, requisitos procesales |
| Inyectables bioestimulantes (muy conservadores) | Estimular el colágeno sin punción epidérmica. | Riesgo de nódulos, requiere inyector experimentado. |
Combinación de microagujas con otras terapias: momento oportuno y seguridad
Si planeo combinar tratamientos, programo la microaguja con al menos varias semanas de diferencia de los procedimientos térmicos o ablativos y consulto con los demás profesionales que me atienden. Una sincronización cuidadosa reduce la inflamación superpuesta y minimiza el riesgo acumulativo para la piel fina.
Cómo elijo un proveedor de microagujas
Busco profesionales con formación médica (dermatólogos, auxiliares médicos o enfermeras con experiencia) que demuestren conocimiento sobre el grosor de la piel, tengan prácticas de esterilización estrictas y adapten los protocolos. También valoro fotos de antes y después de tipos de piel similares y explicaciones claras sobre los planes de contingencia ante complicaciones.
Preguntas que siempre le hago a mi proveedor
Pregunto sobre sus protocolos de esterilización, la profundidad específica de las agujas que planean usar, cómo evalúan la piel fina, el régimen exacto de cuidados posteriores y si realizarán una prueba en una zona específica si tengo factores de riesgo. También pregunto sobre los procedimientos de emergencia y la programación de citas de seguimiento.
Consideraciones de costos y valor
Los costos varían considerablemente según la ubicación, las credenciales del proveedor y si se incluyen complementos como el PRP. Normalmente, valoro el precio y la experiencia del proveedor en lugar de buscar la opción más económica. Para pieles delicadas, estoy dispuesto a pagar más por un profesional con experiencia, ya que una técnica cuidadosa y un seguimiento adecuado reducen los costos y las complicaciones posteriores.
Expectativas realistas que establezco para los resultados
Les digo a las personas que la microaguja puede mejorar las líneas de expresión, la textura y las cicatrices superficiales, pero los resultados son graduales y dependen de la biología de la piel y de la adherencia al cuidado posterior. Para pieles finas, enfatizo objetivos modestos: mejorar la textura y el tono sin cambios agresivos que puedan comprometer la barrera cutánea.
Cuándo detener o pausar el tratamiento
Si después de una sesión noto enrojecimiento persistente, retrasos repetidos en la cicatrización o capilares rotos que se extienden, suspendo los tratamientos posteriores y reevalúo la situación. También los detengo si existe un problema médico agudo que pueda afectar la cicatrización, como el uso de esteroides sistémicos o un nivel de azúcar en sangre descontrolado.
Mi lista de verificación práctica antes de reservar una sesión
Me aseguro de revelar todo mi historial médico, suspender los tópicos irritantes a tiempo, confirmar las credenciales de mi profesional y su práctica de esterilización, y coordinar un cuidado posterior adecuado (descanso, uso de productos suaves). También planeo documentar el estado inicial de mi piel con fotos para monitorear los cambios.
Veredicto final: ¿Es segura la microaguja para la piel fina?
Creo que la microaguja puede ser segura para pieles finas cuando se realiza de forma conservadora por profesionales con experiencia que adaptan la profundidad, el espaciado y los cuidados posteriores al riesgo individual. Sin embargo, también reconozco que la piel fina aumenta la sensibilidad a las complicaciones, por lo que una evaluación cuidadosa, un entorno conservador y un cuidado posoperatorio estricto son esenciales.
Preguntas frecuentes
¿La microaguja puede empeorar la piel fina?
Sí. Si se realiza de forma demasiado agresiva o sin tener en cuenta las características de la piel fina, la microaguja puede prolongar el enrojecimiento, causar hematomas o, en raras ocasiones, dejar cicatrices. Insisto en los protocolos suaves y el tratamiento por etapas para minimizar ese riesgo.
¿Puede la microaguja causar daños permanentes en la piel fina?
El daño permanente es poco común, pero es posible si hay infección, mala cicatrización o una profundidad y frecuencia inadecuadas. Reduzco ese riesgo detectando contraindicaciones y supervisando de cerca la cicatrización.
¿Es segura la microaguja con PRP para pieles finas?
El PRP puede mejorar la cicatrización, pero la combinación de microagujas con PRP en piel fina debe ser realizada por profesionales con experiencia en ambos procedimientos. Quiero que el PRP se aplique en condiciones estériles y probablemente usaría una menor profundidad para reducir el trauma mecánico.
¿Es seguro utilizar un dermaroller en casa si mi piel es fina?
Generalmente no recomiendo los derma rollers caseros para pieles finas debido a la higiene, la presión descontrolada y la calidad variable de las agujas. Si alguien insiste, establezco límites estrictos: agujas muy superficiales, esterilización impecable y suspensión inmediata en caso de enrojecimiento excesivo.
¿Cuánto tiempo pasará hasta que vea mejoras?
Es posible que se observe cierta mejora en la textura en cuestión de semanas, pero la mayoría de las personas notan resultados significativos tras una serie de 3 a 6 sesiones a lo largo de varios meses. Recomiendo la paciencia y un cuidado posterior constante para que el colágeno se regenere.
¿La microaguja reducirá la delgadez o realmente engrosará mi piel?
La microaguja estimula la producción de colágeno y puede aumentar ligeramente el grosor dérmico con el tiempo, pero no restaurará drásticamente el tejido perdido en una sola sesión. Recomiendo objetivos realistas: una mejora gradual en lugar de la reversión total de un adelgazamiento severo.
¿Qué pasa si estoy tomando esteroides tópicos o los he usado recientemente?
Los esteroides tópicos y sistémicos pueden debilitar la piel y dificultar la cicatrización; prefiero un intervalo sin esteroides y, en ocasiones, una consulta con un dermatólogo antes de continuar. Si el tratamiento con esteroides continúa por una razón médica, me coordino con el médico que lo prescribe.
¿Cómo debo proteger mi piel inmediatamente después del tratamiento?
Utilizo un limpiador suave, una crema hidratante suave y protector solar físico una vez que la piel deja de supurar; evito los ingredientes activos hasta que la piel esté completamente curada. También evito el maquillaje durante al menos 24 a 48 horas, según las instrucciones del profesional.
¿Puede la microaguja ayudar con los vasos sanguíneos visibles y la translucidez?
La microaguja puede reducir la apariencia de las líneas de expresión y mejorar la textura, pero los vasos sanguíneos visibles suelen tratarse mejor con terapias dirigidas a los vasos sanguíneos, como el láser de colorante pulsado o la luz pulsada intensa (IPL). A veces combino enfoques, pero los tratamientos vasculares deben elegirse con cuidado para la piel fina.
¿Cuándo debo buscar atención médica después de la microaguja?
Busco atención urgente si observo enrojecimiento que se extiende, aumento del dolor, pus, fiebre o signos de infección sistémica. Si el enrojecimiento, la hiperpigmentación o las cicatrices persisten, consulto con un dermatólogo para obtener intervenciones específicas.
Espero que esto te brinde un marco claro y práctico para decidir si la microaguja es adecuada para pieles finas. Si lo deseas, puedo ayudarte a preparar una lista de preguntas para llevar a la consulta o guiarte por una lista de verificación de riesgos individualizada según tu historial médico y examen de la piel.